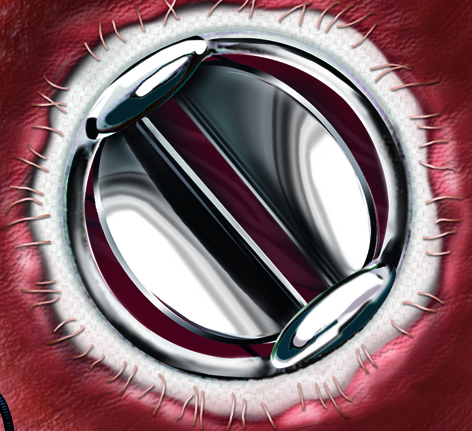
Patienten mit künstlichem Herzklappenersatz
Bei Menschen über 65 Jahren in der EU hat ca. einer von 20 eine Verengung der Aortenklappe, ca. 0,2 % der Menschen haben eine künstliche Herzklappe, in 75 % der Fälle handelt es sich um eine künstliche Aortenklappe, seltener werden Mitralklappen ersetzt oder auch beide Klappen.
Ohne die Anwendung einer Gerinnungshemmung würde bei Patienten mit künstlichem Herzklappenersatz bei ca. 86 von 1000 Patienten eine Thromboembolie (z.B. Schlaganfall) und bei ca. 18 von 1000 Patienten eine Klappenthrombose auftreten. Die Gerinnungshemmung reduziert die Rate der Thromboembolien um etwa 80 %, die der Klappenthrombosen um etwa 90 %.1,2 Der Nutzen der Gerinnungshemmung überwiegt daher das Blutungsrisiko bei weitem.

Patienten mit Vorhofflimmern (VHF)
Das VHF ist die häufigste Herzrhythmusstörung. Bei ca. 25 % der jetzt 40-jährigen Patienten wird im weiteren Lebensverlauf VHF auftreten. VHF geht mit einem 5-fach erhöhten Schlaganfallrisiko einher. Konkret bedeutet dies, dass bei ca. 5 % der Patienten mit VHF/Jahr ein Schlaganfall auftritt. Die Schlaganfälle bei Patienten mit VHF sind leider besonders schwerwiegend und haben daher ein hohes Risiko für schwere Behinderung oder Tod, etwa 30 - 50 % der Patienten mit VHF und Schlaganfall versterben daher 3. Bei 20 - 30 % der Patienten mit Schlaganfall wird wiederum erstmals ein VHF gefunden. Die Einnahme von Gerinnungshemmern senkt die Schlaganfallrate erheblich um ca. 64 % 4.
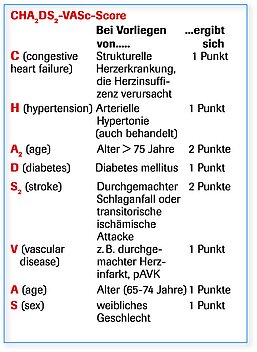
Ob ein Patient mit Gerinnungshemmung behandelt werden sollte, hängt neben dem VHF von weiteren Risikofaktoren ab. Diese werden im sog. CHA2DS2-VASc-Score erfasst, die Punktzahl dient dann der Entscheidungsfindung, (Abb. 1). Gleichzeitig wird versucht, das Blutungsrisiko unter Gerinnungshemmung zu erfassen mit dem sog. HAS-BLED-Score, (Abb. 2). Diese Daten zusammengenommen führen dann zur Entscheidungsfindung. Die Erfahrung lehrt, dass der Großteil der Patienten mit VHF, ca. 80 - 90 %, von der Gerinnungshemmung profitieren 5. Nur bei Patienten mit sehr geringen Risikofaktoren kann ggf. auch Aspirin (ASS 100) ausreichen.
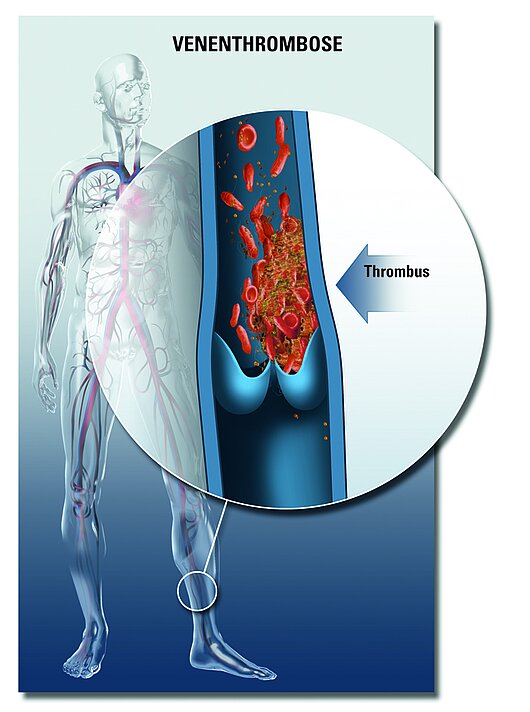
Patienten mit tiefen Thrombosen/Lungenembolien
Die Häufigkeit der Thrombosen/Lungenembolien liegt in Europa bei ca. 3 - 4 Fälle auf 1000 Einwohner/Jahr. Das Risiko ist stark vom Lebensalter abhängig und steigt insbesondere ab 40 Jahren an, bei über 65-jährigen liegt die Häufigkeit schon bei ca. 14 Fällen auf 1000 6.
Als Risikofaktoren für Thrombosen/Embolien gelten neben dem Lebensalter:
- Genetische Veranlagung (= Thrombophilie)
- Medikamente (v.a. Östrogene, Kortison)
- Immobilität (Verletzung, OP, lange Flug-/Autoreise)
- Flüssigkeitsverlust
- Tumorerkrankungen
- große Operationen
- Schwangerschaft
So kann bei Vorliegen einer genetischen Veranlagung eine Thrombose/Embolie auch bereits bei jungen Menschen auftreten, z. B. nach OP oder unter Östrogeneinnahme.
Nach Diagnose einer Thrombose/Embolie muss sofort eine ausreichende Gerinnungshemmung eingeleitet werden, um ein Thrombuswachstum und eine Lungenembolie (Abschwimmen des Thrombus meist aus dem Bein in die Lunge) zu verhindern. Das Risiko der Lungenembolie fällt sofort nach Beginn der Gerinnungshemmung nahe gegen Null.
Da der Körper längere Zeit braucht, um die Gefäße wieder durchgängig zu kriegen, muss die Gerinnungshemmung je Art und Lokalisation der Thrombose ca. 3- 12 Monate fortgesetzt werden.
Bestehen so starke Risikofaktoren, dass eine hohes Wiederholungsrisiko für eine Thrombose besteht, wird in Einzelfällen auch eine lebenslange Blutgerinnungshemmung empfohlen.
Generell wird also bei allen o.g. Patientengruppen eine Einschätzung vorgenommen, ob das Risiko für Gefäßverschluss das Komplikationsrisiko der Gerinnungshemmung, und hier v.a. das Blutungsrisiko, überwiegt.
Das Risiko für schwere Blutungen unter Vitamin-K-Antagonisten (z.B. Phenprocoumon) liegt pro Patientenjahr und je nach Patientengruppe bei etwa 1 - 3 % 7.
Dr. med Hannelore Rott, Fachärztin für Transfusionsmedizin; Gerinnungszentrum Rhein-Ruhr; Königstr. 13, D-47051 Duisburg; E-Mail:hannelore.rott@gzrr.de

Literatur
- Whitlock RP. Antithrombotic and Thrombolytic Therapy for Valvular DiseaseAntithrombotic Therapy for Valvular DiseaseAntithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. CHEST. 2012;141(2_suppl):e576S. doi:10.1378/chest.11-2305.
- Misawa Y. Valve-related complications after mechanical heart valve implantation. Surgery Today. April 2015:1-5. doi:10.1007/s00595-014-1104-0.
- You JJ. Antithrombotic Therapy for Atrial FibrillationAntithrombotic Therapy for Atrial FibrillationAntithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. CHEST. 2012;141(2_suppl):e531S. doi:10.1378/chest.11-2304.
- Hart RG, Pearce LA, Aguilar MI. Meta-analysis: antithrombotic therapy to prevent stroke in patients who have nonvalvular atrial fibrillation. Ann Intern Med. 2007;146(12):857-867.
- Trappe H-J. Atrial fibrillation: established and innovative methods of evaluation and treatment. Deutsches Ärzteblatt International. 2012;109(1-2):1-7. doi:10.3238/arztebl.2012.0001.
- ISTH Steering Committee for World Thrombosis Day. Thrombosis: A major contributor to global disease burden. Thromb Haemost. 2014;112(5):843-852. doi:10.1160/TH14-08-0671.
- Lip GYH, Keshishian A, Kamble S, et al. Real-world comparison of major bleeding risk among non-valvular atrial fibrillation patients initiated on apixaban, dabigatran, rivaroxaban, or warfarin. Thromb Haemost. 2016;116(5):975-986. doi:10.1160/TH16-05-0403.
